- TRSET
Solüsyon nedir? İdeal bir solüsyon elde etmek için karışım oranı nasıl saptanır?
Çözeltiler kaça ayrılır? Bir çözeltideki karışım oranı nasıl hesaplanır?
Homojen karışımlara ne ad verilir? Heterojen karışımlar çözelti midir? #Kimya #Solut
+ index service
+ TR Search Engine Technology
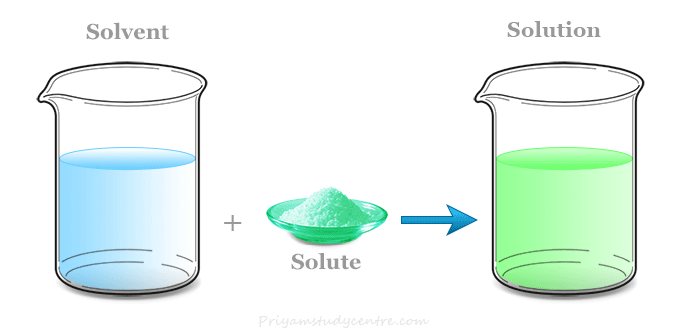
Çözelti / Solüsyon
En az iki maddenin herhangi bir oranda bir araya gelerek oluşturdukları homojen karışımlara çözelti ya da solüsyon adı verilir. Diğer bir deyişle; bir maddenin başka bir madde içinde gözle görülemeyecek kadar küçük tanecikler halinde dağılarak (homojen) bir karışım oluşturmasına çözünme ve elde edilen karışıma ise çözelti denilmektedir.
Bir çözeltiyi oluşturan maddelerden yüksek miktarda olanına çözücü, az olanına ise çözünen adı verilir. Evrende birçok çözücü ve çözünen madde vardır. Mevcut teknolojimize dayanarak söyleyebiliriz ki; doğadaki en iyi çözücü sudur. Genelde çoğu katı, sıvı ve gaz maddeler suda çözünürler. Gazoz, çay, deniz suyu, limonata, mürekkepli su, alkollü su, şekerli su çözeltiye örnek olarak verilebilir.
Çözünme olayı erime ile karıştırılsa da ikisi de farklı eylemlerdir. Çözünmede dışarıdan bir ısı desteğine ihtiyaç yoktur.

Çözelti türleri üç ana başlık altında toplanabilir:
- Çözücünün fiziksel haline göre :
- katı, sıvı, gaz
- İletkenliklerine göre :
- İyonik / Elektrolit Çözeltiler : çözünen madde çözünürken iyonlarına ayrılıyorsa elektrik akımını iletir. Örneğin tuzlu su ( tuz suda Na+ ve Cl- olarak ayrışır)
- Yalıtkan Çözeltiler : kovalent bağlı bileşikler çözücü madde içerisinde moleküllerine ayrılarak çözünür. Mesela alkollü su bu nedenle elektrik akımını iletmez.
- Çözünen madde miktarına göre :
- Doymuş Çözeltiler : çözücünün çözebileceği maksimum maddeyi çözebildiği durunlara denir.
- Aşırı Doymuş Çözeltiler: çözeltinin azami (maksimum) çözebileceği madde miktarından daha fazla madde çözünmüş durumdaki çözeltilerdir ve kararsız yapıdadırlar. Bu çözeltilerde bir miktar çözünen madde çökerek doymuş çözelti haline gelir.
- Doymamış Çözeltiler : bir çözücünün çözebileceği azami (maksimum) maddeden daha azını çözdüğü durumlardır. Bu tür çözeltilere belli bir miktar daha çözünen eklendiği zaman çözücü, eklenen çözüneni de çözebilir.
- Seyreltik Çözeltiler : çözünenin az olduğu çözeltilerdir. Birim hacme düşen çözünen madde miktarı ne kadar azsa çözelti o kadar seyreltiktir.
- Derişik Çözeltiler : çözünen miktarının çok olduğu çözeltilerdir. Birim hacme düşen çözünen madde miktarı ne kadar çoksa çözelti o kadar derişiktir.
Çözeltide çözünmüş olarak bulunan madde miktarına derişim ya da konsantrasyon denir.

Son olarak konuyu artık bağlayalım :)
Titre / Ayarlı / Titrant / Standart Çözeltiler
Asit ya da baz derişimi bilinen ve bu sayede titrasyonda kullanılabilen çözeltilere titre çözelti denir.
- Normal Çözeltiler
- Molar Çözeltiler
- Ozmolar Çözeltiler
- İzotonik Çözeltiler
- Hipotonik Çözeltiler
- Hipertonik Çözeltiler
- Standart Çözeltiler
Normal Çözeltiler
1 litresinde 1.008 g (1 atom gram) H+ bulunan çözeltilere normal asit çözeltisi , 17.008 g OH- bulunan çözeltilere de normal baz çözeltisi denir.
Çözeltide mevcut H+ ve OH- iyonları miktarının arttığı / azaldığı oranda normalite de artar veya azalır (5 N veya 0.3 N gibi) .
Normalite N ile gösterilir. Bir maddenin 1 N çözeltisi, 1 Litresinde o maddenin 1 eşdeğer gramını (yani ekivalan gram) içeren çözelti demektir.
Eşdeğer gram = Molekül gram / değerlik
Video : Murat YILDIZ

-

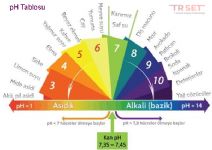 pH Dengesi, Asit, Baz ve Sulu Çözelti Dengeleri
pH Dengesi, Asit, Baz ve Sulu Çözelti Dengeleri -

 Elektroliz Nedir?
Elektroliz Nedir? -

 Kimyasal Karışımlar. Karışım Nedir?
Kimyasal Karışımlar. Karışım Nedir? -

 Asetik Asit Nedir?
Asetik Asit Nedir? -

 Kimyada Bileşikler Nasıl Adlandırılır?
Kimyada Bileşikler Nasıl Adlandırılır? -

 Entalpi, HESS Yasası ve Bağ Enerjisi
Entalpi, HESS Yasası ve Bağ Enerjisi -

 Le Chatelier Prensibi
Le Chatelier Prensibi -

 Mol nedir? Avogadro nedir? Herkes için anlaşılır kimya konuları.
Mol nedir? Avogadro nedir? Herkes için anlaşılır kimya konuları. -

 Atom ve Periyodik Sistem
Atom ve Periyodik Sistem
-
Modern Fiziğin Teknolojideki Uygulama Alanları
-
Kimyasal Karışımlar. Karışım Nedir?
-
Solunum Sistemi
-
Statik Elektrik Nedir ?
-
Çınar 77 Zemin, Fore Kazık, Güçlendirme ve Sondaj Sistemleri
-
Dinamometre : Kuvvet Ölçer
-
pH Dengesi, Asit, Baz ve Sulu Çözelti Dengeleri
-
24 Mayıs Tarihte Bugün
-
Kimyada Bileşikler Nasıl Adlandırılır?

 Bu Sayfayı Paylaş
Bu Sayfayı Paylaş WhatsApp CH
WhatsApp CH Twitter
Twitter YouTube
YouTube Linked in
Linked in Instagram
Instagram Facebook
Facebook Türkçe
Türkçe Deutsch
Deutsch English
English